आमतौर पर एक नई बीमारी की खोज और उसके कारण का पता लगाने के बीच दशकों, कभी-कभी सदियों लगते हैं, एक नई ऑटोइंफ्लेमेटरी बीमारी (CRIA) का अभी फिलहाल पता चला है जो कि हमारी प्रतिरक्षा प्रणाली (Immune System) को कमजोर करती है, जिस रिसर्च पेपर में इस बीमारी (Swollen Lymph Nodes) के बारे में वर्णन किया गया है उसी पेपर में इसके उपचार का भी वर्णन है।
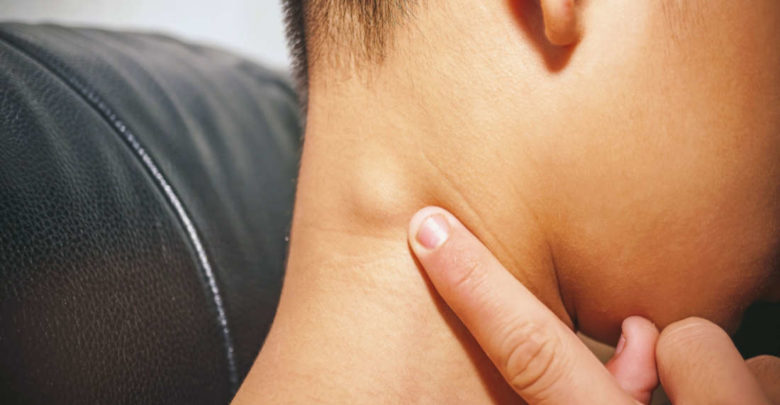
एक आनुवंशिक उत्परिवर्तन (genetic mutation) कभी-कभी कुछ लोगों में अत्यधिक बुखार और दर्द के लगातार प्रकोप का कारण बनता है। इसकी वजह से लिम्फ ग्रंथियां (Swollen Lymph Nodes) सूज जाती हैं और अन्य असामान्य लक्षण पैदा हो सकते हैं। जिस टीम ने इसपर अपना शोध किया है उनका मानना है कि उन्होंने जो सीखा है, वह ऑटोनोफ्लेमेटरी बीमारी के अन्य रूपों की हमारी समझ को बेहतर बनाएगा,जिससे व्यापक रूप से लाभ बहुत लोगों को मिलेगा।
नेशनल ह्यूमन जीनोम रिसर्च इंस्टीट्यूट के डॉ दान कस्तनर को “ऑटोनोफ्लेमेटरी बीमारी के जनक” के रूप में जाना जाता है, जिन्होंने इन खराब समझ वाली स्थितियों की हमारी अज्ञानता को दूर करने के लिए बहुत कुछ किया है। Kastner का ध्यान उन लोगों पर अधिक गया जो हर 2-4 सप्ताह में बीमार हो जाते हैं, कभी -कभी ये एक दिन तो कभी ये एक पूरे सप्ताह के लिए बीमार ही रहते हैं। लिम्फ ग्रंथियों के सूजने (Swollen Lymph Nodes) के अलावा भी इसमें लिवर का बढ़ना और मुँह के छाले दिखना ये सभी लक्षण सामने आते ही रहते हैं। जन्म से लेकर के बुढ़ापे तक ये सता सकते हैं और अपने आप कभी नहीं खत्म होते, एक रोगी जो कि अपने 80वें वर्ष में है उसे आज भी इन चीजों से समाना करना पड़ता है।
Kastner ने जिन तीन परिवारों का अध्ययन किया, उनमें यह संकेत मिलता है कि यह आनुवांशिक (Genetic) है, और परीक्षण से पता चला कि RIPK1 जीन (Gene) पर इसके सभी उत्परिवर्तन (Mutations) होते हैं। RIPK1 जीन पर अभी हाल में ही कई वैज्ञानिकों का ध्यान केंद्रित हुआ है, ये सोचकर कि ये जीन कई स्थितियों में महत्वपूर्ण हो सकता है, इसलिए Kastner ने डॉ नजारा ललौई सहित वाल्टर और एलिजा हॉल इंस्टीट्यूट में RIPK1 विशेषज्ञों की एक टीम के साथ संपर्क किया है।
विज्ञान पत्रिका नेचर में ललौई और उनके साथियों ने इस बीमारी को cleavage-resistant RIPK1-induced autoinflammatory (CRIA) syndrome नाम दिया है, जो कि सैल्स की मृत्यु का कारण बन सकती है, या जब होती है तो सैल डैथ चालू हो जाती है।
सैल्स की मृत्यु का ये रास्ता या सेैल डैथ पाथवे इनबिल्ट मैकेनिज्म की एक ऐसी श्रृंखला विकसित करता है जो जो भड़काऊ संकेतों (inflammatory signals) और सेल डेथ को नियंत्रित करती है। डाॅ ललौई आगे कहती हैं कि इस बीमारी में जो RIPK1 Gene पर जो उत्परिवर्तन होते हैं वो सभी सामान्य जांचों और नियंत्रण को भी पार करके अनयिंत्रित सैल डेथ और यानि कोशिकाओं की मृत्यु और सूजन को बढ़ावा देते हैं।
हैरानी इस बात की है जिन तीनों परिवारों पर ये सोध हुआ है वो सभी अलग-अलग RIPK1 Gene की उत्परिवर्तन (Mutations) को दिखाते हैं, पर इसके बाद भी जो बीमारी के लक्षण हम देखते हैं वो तीनों ही केश में एक जैसे ही होते हैं, इसमें RIPK1 प्रोटीन को तोड़ने या उसे विभाजित करने पर पाबंदी लग जाती है जिससे ये लक्षण उभर जाते हैं।
Lalaoui आगे समझाते हुए कहती हैं कि भले ही इस बीमारी से हमारी कोशिकायें मरने लग जाती हों पर इसका प्रभाव केवल कुछ ही जगहों पर होता है पूरे शरीर पर कभी नहीं होता। ज्यादातर इस बीमारे से हमारी लिम्फ ग्रंथियां सूज (Swollen Lymph Nodes) जाती है जिससे हमें काफी कठिनाई अनुभव होने लगती है। कुछ दवाइयां इन लक्षणों को दवाने में मदद करती हैं पर वे इतनी असरदार नहीं हैं कि इन्हें पूरी तरह से ठीक कर सकें।
इस बीच, लालाओई ने कहा, इस खोज से ऑटोनोफ्लेमेटरी स्थितियों की एक श्रृंखला में कोशिका मृत्यु के महत्व को अधिक से अधिक मान्यता मिल सकती है, फिलहाल RIPK1 जीन की म्यूटेशन को रोकने के लिए कई तरह के RIPK1-inhibitors पर काम हो रहा है पर वे अभी भी अपनी पहली स्टेज पर हैं।